Hcl Nedir
Hidroklorik asit, güçlü ve yüksek çözünürlüğe sahip bir asittir. Molekül yapısı basittir; bir hidrojen (H) ve bir klor (Cl) atomundan oluşur ve formülü HCl’dir. Hidrojen klorür gazı, oda sıcaklığında suda çözündüğünde yaklaşık 450 litre çözeltide çözünür ve tamamen iyonlaşarak güçlü bir asit oluşturur. Bu özellikleri sayesinde hem endüstride hem laboratuvarlarda geniş kullanım alanına sahiptir.
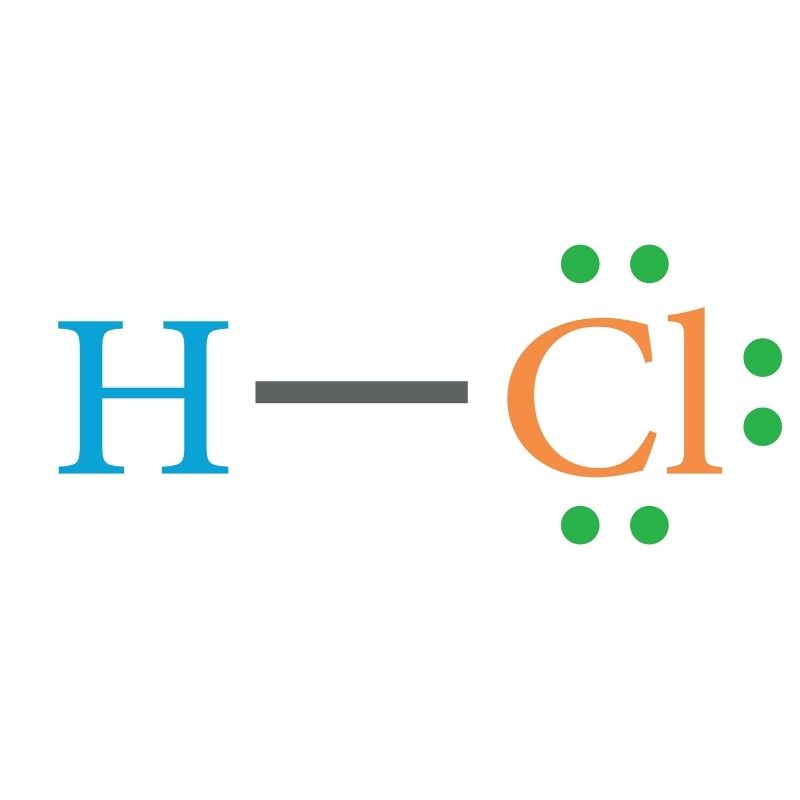
HCl Formülü Nedir?
HCl formülü, bir hidrojen (H) ve bir klor (Cl) atomundan oluşan kimyasal bileşiği ifade eder. Bu bileşik gaz halinde hidrojen klorür, su içinde çözündüğünde ise hidroklorik asit adını alır.
HCl iki atomlu (diatomik) bir moleküldür ve yapısında yalnızca 1 adet hidrojen ve 1 adet klor atomu bulunur. Bu iki atom arasında polar kovalent bağ vardır. Klor atomu hidrojene göre daha elektronegatif olduğu için bağ elektronlarını kendine doğru çeker ve bu durum molekülün kutuplu (polar) olmasına neden olur.
Kimyasal özellikleri:
- Kimyasal formül: HCl
- Molekül tipi: İki atomlu (diatomik)
- Bağ türü: Polar kovalent bağ
- Molekül geometrisi: Doğrusal
Gaz ve Sulu Hali:
- Gaz haldeyken: Hidrojen klorür (HCl)
- Su içinde çözündüğünde: Hidroklorik asit adını alır ve güçlü asidik özellik gösterir.

HCl Açılımı Nedir?
HCl’nin açılımı Hidrojen Klorürdür. Formülde yer alan H hidrojen atomunu, Cl ise klor atomunu temsil eder. Bu iki element birleşerek iki atomlu (diatomik) bir bileşik oluşturur. Gaz halinde bulunduğunda kimyasal adı hidrojen klorürdür.
HCl Yaygın Adı Nedir?
HCl’nin su içindeki çözeltisinin kimyasal adı hidroklorik asittir. Günlük hayatta ve temizlik ürünlerinde ise yaygın olarak tuz ruhu adıyla bilinir. Özellikle kireç çözücü ve yüzey temizleyici olarak kullanıldığı için bu isimle tanınır.
HCl Asit mi Baz mı?
HCl bir asittir. Su içinde çözündüğünde hidrojen iyonu (H⁺) vererek çözeltinin asidik olmasına neden olur. Bu nedenle güçlü asitler sınıfında yer alır.
- pH değeri düşüktür (konsantrasyona bağlı olarak 0–1’e kadar inebilir).
- Bazlarla tepkimeye girerek tuz ve su oluşturur.
- Metalleri aşındırıcı etki gösterebilir.
Özetle HCl baz değil, sulu ortamda güçlü asidik özellik gösteren bir bileşiktir.
HCl Özellikleri Nelerdir?
Hidrojen klorür, bir hidrojen (H) ve bir klor (Cl) atomundan oluşan iki atomlu (diatomik) bir moleküldür. Normal koşullarda renksiz, keskin kokulu ve tahriş edici özellikte bir gazdır. Havadan daha ağırdır ve nemli ortamlarda su buharıyla temas ettiğinde beyaz asidik duman oluşturur.
Molekül yapısı doğrusal (linear) olup H–Cl bağı polar kovalent bağdır. Bunun nedeni klor atomunun hidrojenden daha yüksek elektronegatifliğe sahip olmasıdır. Elektron yoğunluğu klor tarafına kayar ve molekülde kısmi yük farkı oluşur. Bu durum HCl’nin polar bir molekül olmasına yol açar.
Fiziksel özellikleri:
- Kaynama noktası yaklaşık −85 °C
- Erime noktası yaklaşık −114 °C
- Suda çözünürlüğü çok yüksektir
Kimyasal olarak oldukça reaktiftir. Suya geçtiğinde tamamen iyonlaşarak güçlü bir asit oluşturur. Bazlarla nötrleşme tepkimesi verir, aktif metallerle reaksiyona girerek hidrojen gazı çıkarabilir ve karbonatlarla karbondioksit gazı oluşturur. Bu özellikleri nedeniyle hem endüstride hem laboratuvar ortamında yaygın olarak kullanılır.
HCl pH Değeri Kaçtır?
Gaz halindeki HCl için pH kavramı geçerli değildir. Çünkü pH yalnızca sulu çözeltiler için tanımlanır. Ancak HCl su içinde çözündüğünde hidroklorik asit oluşturur ve bu durumda pH değeri ölçülebilir.
HCl → H⁺ + Cl⁻
Bu tam iyonlaşma özelliği, HCl’yi güçlü asit yapar. Seyreltik çözeltilerde pH değeri genellikle 1–2 aralığındadır. Daha konsantre çözeltilerde ise pH 0’a yaklaşabilir hatta teorik olarak 0’ın altına düşebilir.
pH değeri çözeltinin derişimine bağlıdır. Derişim arttıkça hidrojen iyonu (H⁺) miktarı artar ve pH daha da düşer. Bu düşük pH seviyesi, hidroklorik asidin aşındırıcı ve korozif özellik göstermesine neden olur. Bu nedenle özellikle yüksek konsantrasyonlu çözeltiler dikkatle kullanılmalıdır.
HCl Polar mı Apolar mı?
HCl molekülü polardır.
Bunun nedeni hidrojen ve klor arasındaki elektronegatiflik farkıdır. Klor atomu elektronları kendine daha güçlü çektiği için bağ elektronları klor tarafına kayar.
- Hidrojen ucu kısmi pozitif (+)
- Klor ucu kısmi negatif (−)
Molekül doğrusal olmasına rağmen yük dağılımı simetrik değildir. Bu nedenle molekülün net bir dipol momenti vardır. Bu dipol moment, HCl’nin su gibi polar çözücülerde kolay çözünmesini sağlar.
Ayrıca polar yapısı sayesinde su molekülleriyle güçlü etkileşim kurar ve suda tamamen iyonlaşarak güçlü asit davranışı gösterir. Eğer apolar olsaydı bu kadar yüksek çözünürlük ve tam iyonlaşma görülmezdi.
HCl Nasıl Elde Edilir?
Hidrojen klorür (HCl) hem laboratuvar ortamında hem de endüstriyel ölçekte çeşitli yöntemlerle elde edilebilir. Elde edilme yöntemi kullanım amacına ve üretim miktarına göre değişiklik gösterir.
Endüstride en yaygın üretim yöntemi, hidrojen gazı (H₂) ile klor gazının (Cl₂) doğrudan reaksiyonudur:
H₂ + Cl₂ → 2HCl
Bu reaksiyon oldukça ekzotermiktir, yani yüksek miktarda ısı açığa çıkarır. Kontrollü ortamda gerçekleştirilir çünkü klor gazı zehirli, hidrojen gazı ise yanıcıdır. Reaksiyon sonucunda elde edilen ürün gaz halde hidrojen klorürdür.
Bir diğer yöntem, organik kimya süreçlerinde yan ürün olarak ortaya çıkmasıdır. Özellikle PVC üretimi gibi klor içeren bileşiklerin sentezinde HCl gazı yan ürün olarak açığa çıkar.
Laboratuvar ortamında ise genellikle sodyum klorür (NaCl) ile sülfürik asidin (H₂SO₄) reaksiyonu kullanılır:
NaCl + H₂SO₄ → NaHSO₄ + HCl
Bu yöntemde oluşan HCl gazı su içinde çözündürülerek hidroklorik asit elde edilir. Elde edilen gaz doğrudan kullanılabilir ya da suya emdirilerek sıvı formda güçlü bir asit çözeltisi hazırlanır. Üretim sırasında mutlaka gaz kontrol sistemleri ve uygun havalandırma kullanılmalıdır.
Günlük Hayatta Nerede Karşımıza Çıkar?
HCl doğrudan gaz formunda günlük hayatta karşımıza çıkmaz; ancak çözeltisi olan hidroklorik asit birçok alanda kullanılır.
En bilinen örnek mide asididir. İnsan midesinde bulunan asidin temel bileşeni hidroklorik asittir. Bu asit besinlerin sindirilmesine yardımcı olur, proteinleri parçalar ve zararlı mikroorganizmaları öldürür.
Temizlik ürünlerinde de hidroklorik asit yaygındır. Özellikle kireç çözücü ve tuz ruhu olarak bilinen ürünlerde bulunur. Banyo ve tuvalet temizliğinde kullanılır çünkü kalsiyum karbonatı hızlı şekilde çözer.
Ayrıca metal yüzey temizleme işlemlerinde, pas giderme uygulamalarında, havuz pH ayarlamalarında ve deri ile tekstil sanayisinde karşımıza çıkar. Ancak yüksek korozif özelliği nedeniyle bilinçsiz kullanım ciddi yanıklara ve solunum yolu tahrişine neden olabilir.
Su İçinde Çözündüğünde: Hidroklorik Asit (HCl Çözeltisi)
HCl gazı su içinde çözündüğünde hidroklorik asit oluşur. Bu çözünme basit bir fiziksel olay değildir; kimyasal iyonlaşma gerçekleşir.
HCl + H₂O → H₃O⁺ + Cl⁻
Burada hidrojen iyonu serbest halde bulunmaz, su molekülüne bağlanarak hidronyum (H₃O⁺) oluşturur. Bu iyonlaşma neredeyse %100’dür. Bu nedenle hidroklorik asit güçlü asit sınıfına girer.
Renksiz ve keskin kokulu bir sıvıdır. Yüksek derecede koroziftir. Metallerle reaksiyona girebilir ve bazlarla nötrleşme tepkimesi verir. Özellikleri çözeltinin derişimine bağlıdır. Seyreltik çözeltiler daha az tehlikeliyken, konsantre çözeltiler ciddi kimyasal yanıklara neden olabilir.
Hidroklorik Asit Ne İşe Yarar?
Hidroklorik asit hem biyolojik hem de endüstriyel açıdan önemli görevler üstlenir. İnsan vücudunda mide asidi olarak görev yapar. Proteinleri denatüre eder, sindirim enzimlerinin aktifleşmesini sağlar ve zararlı mikroorganizmaları yok eder.
Endüstride ise metal yüzey temizliği, pas giderme, kimyasal üretim süreçleri, pH ayarlama ve iyon değişim reçinelerinin yenilenmesi gibi alanlarda kullanılır. Ayrıca plastik, boya, ilaç ve gübre üretiminde ara madde olarak görev alır.
Hidroklorik Asit Nerelerde Kullanılır?
Hidroklorik asit (HCl çözeltisi), hem endüstride hem de laboratuvar ortamlarında çok yaygın bir şekilde kullanılır. Kimyasal özellikleri ve güçlü asidik yapısı sayesinde birçok alanda vazgeçilmezdir. Başlıca kullanım alanları şunlardır:
- Metal temizliği ve pas giderme: Çelik ve demir yüzeylerdeki oksit ve pas tabakalarını çözmek için kullanılır.
- Gıda sanayisi: Asitlik düzenleyici olarak, örneğin mısır şurubu ve jelatin üretiminde yer alır.
- Kimyasal üretim: PVC, vinil klorür, organik kimyasallar ve bazı gübre türlerinin üretiminde ara madde olarak görev yapar.
- Su arıtma: pH kontrolü ve suyun dezenfeksiyonu işlemlerinde kullanılır.
- Laboratuvar kullanımı: Nötrleştirme, titrasyon ve diğer analitik deneylerde sıkça tercih edilir.
Hidroklorik asit ayrıca tekstil, deri ve petrol endüstrilerinde, asidik ortam gerektiren çeşitli proseslerde kullanılır. Kullanım sırasında yüksek konsantrasyonlu çözeltilerde mutlaka uygun güvenlik önlemleri alınmalıdır, çünkü asit cilt, göz ve solunum yolları için ciddi tahriş edici özellik gösterir.
Hidroklorik Asit Görevleri Nelerdir?
Hidroklorik asit, hem biyolojik hem de endüstriyel görevleri olan çok yönlü bir kimyasaldır. Görevleri kullanım alanına göre değişir ve genellikle çözeltinin asidik özelliklerinden faydalanılır. Ana görevleri şunlardır:
- Mide asidi olarak görev: İnsan vücudunda HCl, mide sıvısının temel bileşenidir ve sindirimi kolaylaştırır, proteinleri parçalar, mikroorganizmaları öldürür.
- pH düzenleyici: Endüstride ve su arıtma tesislerinde çözeltilerin asiditesini ayarlamak için kullanılır.
- Pas ve oksit giderici: Metal yüzeylerdeki pas ve oksit tabakasını çözerek temizleme sağlar.
- Kimyasal ara madde: PVC, vinil klorür, gübre ve çeşitli organik kimyasalların üretiminde kullanılır.
- Laboratuvar görevleri: Titrasyon, nötrleştirme ve analitik deneylerde H⁺ iyon kaynağı olarak görev yapar.
Bu görevlerin tümü, HCl’nin güçlü asidik ve iyonlaştırıcı özelliklerine dayanır. Kullanım sırasında mutlaka koruyucu ekipman ve güvenlik önlemleri uygulanmalıdır.
Hidrojen Klorür (HCl) Gazı Nedir?
Hidrojen klorür, HCl formülüne sahip iki atomlu bir gazdır. Normal sıcaklık ve basınçta renksizdir ancak keskin ve boğucu bir kokuya sahiptir.
Havadan daha ağırdır ve nemli ortamda su buharıyla birleşerek beyaz asidik duman oluşturur. Suda çok hızlı çözünür ve çözündüğünde güçlü bir asit meydana getirir.
Solunduğunda üst solunum yollarını tahriş eder ve yüksek konsantrasyonlarda ciddi sağlık riskleri oluşturabilir.
Hidrojen Klorür (HCl) Gazının Terminolojisi
Hidrojen klorür gazı, farklı bağlamlarda çeşitli isimlerle anılabilir. Terminolojisi kullanım amacına ve fiziksel duruma göre değişir. Başlıca terimler şunlardır:
- Hidrojen klorür (HCl gazı): Gaz halinde saf HCl için kullanılan bilimsel isimdir.
- Sulu çözeltisi – Hidroklorik asit: Gazın su içinde çözünmesiyle oluşan güçlü asidik çözeltiyi ifade eder.
- Anhidrit HCl: Susuz, gaz halinde hidrojen klorürü tanımlar.
- Tuz ruhu: Günlük hayatta hidroklorik asit çözeltisine verilen yaygın isimdir.
- Endüstriyel HCl: Sanayi kullanımında yüksek derişimde üretilen HCl çözeltisi veya gazıdır.
Bu terminoloji, kimya ve endüstri literatüründe doğru kullanım ve güvenlik açısından önemlidir.
Hidrojen Klorür (HCl) Gazı Nasıl Tespit Edilir?
Hidrojen klorür gazı, keskin ve boğucu kokusuyla düşük seviyelerde bile fark edilebilir. Ancak profesyonel ve güvenli tespit için özel yöntemler ve cihazlar gerekir. Başlıca tespit yöntemleri:
- Gaz dedektörleri: Ortamda bulunan HCl konsantrasyonunu ppm seviyesinde ölçer ve anlık uyarı verir.
- Kimyasal indikatör tüpleri: HCl ile reaksiyona giren renk değiştirici tüpler kullanılır.
- Laboratuvar analizleri: HCl gazı örnekleri alınarak titrasyon veya spektrofotometrik yöntemlerle miktarı belirlenebilir.
- Taşınabilir sensörler: Endüstriyel alanlarda taşınabilir dedektörlerle güvenli çalışma sağlanır.
HCl gazı tespiti, özellikle endüstriyel ortamlarda kritik öneme sahiptir. Gazın yüksek konsantrasyonları ciddi sağlık riskleri oluşturabileceği için erken tespit ve uyarı sistemleri kullanılır.
Hidrojen Klorür (HCl) Gazı Nerelerde Kullanılır?
Hidrojen klorür gazı doğrudan günlük hayatta çok yaygın olmasa da sanayi ve laboratuvarlarda önemli bir rol oynar. Kullanım alanları şunlardır:
- Kimya endüstrisi: PVC, vinil klorür ve diğer klor içeren organik bileşiklerin üretiminde ara madde olarak kullanılır.
- Metal işlemleri: Metal yüzeylerin pas giderme ve temizleme işlemlerinde, su ile çözünerek hidroklorik asit oluşturur.
- Laboratuvar çalışmaları: Kimyasal sentezler, analitik deneyler ve titrasyonlar için saf gaz veya çözeltisi kullanılır.
- Gıda sanayisi: Doğrudan gaz olarak değil, çözelti formunda pH ayarlama ve bazı işlem aşamalarında kullanılır.
- Sanayi prosesleri: Özel endüstriyel proseslerde, HCl gazı çeşitli kimyasal reaksiyonlarda reaktif olarak görev yapar.
HCl gazı kullanılırken uygun havalandırma, gaz dedektörleri ve kişisel koruyucu ekipmanlarla güvenlik sağlanmalıdır.
Hidrojen Klorür (HCl) Gazının Zararları Nelerdir?
HCl gazı tahriş edici ve korozif özellik gösterir. Solunduğunda boğazda yanma, öksürük, nefes darlığı ve akciğer tahrişi oluşturabilir. Yüksek konsantrasyonda maruziyet akciğer ödemine ve ciddi solunum problemlerine yol açabilir.
Gözle temas ettiğinde şiddetli yanma ve hasar riski vardır. Cilt ile temasında nemle birleşerek asit oluşturur ve kimyasal yanık yapabilir.
Güvenlik Önlemleri Nelerdir?
HCl ile çalışırken mutlaka koruyucu ekipman kullanılmalıdır. Asit dayanımlı eldiven, koruyucu gözlük ve uygun laboratuvar önlüğü gereklidir.
Gaz ortamında çalışılıyorsa uygun havalandırma sistemi ve gaz maskesi kullanılmalıdır. Kaçak tespit sistemleri bulundurulmalı ve kapalı depolama tercih edilmelidir.
Deri teması halinde bol su ile yıkama yapılmalıdır. Göz temasında en az 15 dakika suyla durulama gerekir ve tıbbi yardım alınmalıdır. Depolama sırasında asite dayanıklı kaplar tercih edilmelidir.
Sorumluluk Reddi:
Bu içerik yalnızca bilgi amaçlıdır. HCl (Hidrojen Klorür / Hidroklorik Asit) tehlikeli ve aşındırıcı bir kimyasal maddedir. Evde veya kontrolsüz ortamlarda deney yapmayınız. Üretim, kullanım veya depolama sırasında oluşabilecek zarar, yaralanma veya maddi kayıptan içerik sahibi sorumlu değildir. HCl ile çalışırken mutlaka uygun koruyucu ekipman kullanın ve güvenlik yönergelerine uyun.